La medicina naturale sta compiendo una grande evoluzione. Dalla qualità dell’alimentazione personalizzata, agli integratori come principio attivo, la medicina naturale dopo decenni di sperimentazione, incomincia ad avere delle buone basi sulla biologia delle frequenze, quali regolatrici endogene dei principali processi della fisiologia. La biologia si fonda sull’assunto che lo scambio biochimico è uguale a quello biofisico. E la scienza ha offerto sempre nuove unità di misura per la misurazione dell’energia, anche per le dimensioni vibrazionali, le microcorrenti e i campi elettromagnetici che governano i processi cellulari. Watt, Ampere, Volt, Gauss/Tesla, Angstrom, Decibel, Sievert ecc.…
Lo scienziato Popp ha sancito che i biofotoni, intuiti dai meridiani della medicina cinese e validati scientificamente, presiedono ogni scambio biochimico. Purtroppo non sappiamo ancora come e in che modo. Siamo ancora nella fase dei primi studi clinici. Mentre sugli altri metodi di misurazione sappiamo molto, soprattutto grazie all’esperienza della diagnostica medica che usa sistematicamente l’elettromagnetismo.
Sul piano terapeutico la pratica clinica ha fatto pochi progressi, non utilizzando sistematicamente il grande bagaglio degli studi della medicina nell’archivio mondiale Pubmed.
Oggi sappiamo che il nostro corpo è una rete frequenziale di collegamenti microelettrici, dagli assoni che collegano i neuroni in tutto il corpo attraverso i recettori, alla regolazione cellulare dei potenziali di membrana e di ogni scambio ionico. Se la rete neurale e cellulare è anche elettrica, oltre che chimica, le stesse microcorrenti fisiologiche indotte da stimoli clinici, possono avere effetti riparativi e terapeutici importanti, come ha dimostrato la famosa ma poco conosciuta finestra di risonanza cellulare di Adey del secolo scorso.
L’utilizzo delle onde elettromagnetiche nel corpo umano ha già dei paletti di riferimento clinici importanti, anche se ancora non conosciuti dalle istituzioni sanitarie mondiali e quindi assenti nella formazione degli stessi medici e professioni sanitarie.
Ogni progresso delle fonti di energia dell’umanità, pensiamo alla stessa elettricità o alla scoperta dei raggi X di Curie, ha comportato un prezzo di conoscenza del limite tra danno biologico e beneficio terapeutico e diagnostico. D’altronde si impara solo dall’esperienza, come insegna anche la storia delle grandi epidemie.
Il principio noto in farmacologia e negli integratori, di dose minima efficace, cioè il miglior rapporto tra maggiori benefici clinici e minori effetti collaterali, nell’elettricità e nel magnetismo è ancora sconosciuto.
Sono conosciute le soglie minime di interazione biologica dell’elettricità, magnetismo, non quelle che possono curare senza effetti collaterali significativi. Ad esempio la soglia dei 100 microtesla dei campi elettromagnetici del secolo scorso, limite oltre il quale si potevano avere effetti biologici, risulta assurda e preclude ogni attività clinica terapeutica, dato che è di poco superiore al magnetismo terrestre. Tra l’altro nelle abitazioni elettrificate si raggiungono mediamente campi elettromagnetici vicini ai 200 microtesla quando funzionano gli elettrodomestici. L’asciugacapelli e lo scaldaletto elettrico dovrebbero essere regolamentati perché sparano potenze importanti su ogni millimetro quadro del nostro corpo.
Si sa che il consumo deve essere senza limiti, in ogni campo.
Ogni fatto è questione di equilibrio. I Campi elettromagnetici per essere efficaci oggi, in un ambiente inquinato, devono avere secondo i principi della finestra di risonanza di Adey, un segnale un po’ più forte del livello ambientale, per avere efficacia terapeutica. Questo misurando gli effetti collaterali.
I campi elettromagnetici servono anche (in intensità e frequenza specifiche) a mantenere l’equilibrio naturale e a stimolare l’effetto riparativo biologico.
Ad esempio oggi quasi tutti i dispositivi di magnetoterapia e campi elettromagnetici pulsati usano solo l’onda quadra che serve esclusivamente per la rigenerazione e il dolore osseo. L’onda sinusoidale, naturale e madre di tutte le forme di onda, ha effetti riequilibranti su tante patologie, senza gli effetti collaterali dell’onda quadra che può determinare aritmie, agitazione e altro. I muscoli tra l’altro rispondono solo all’onda sinusoidale, sia le contratture che il dolore muscolare. Questa forma d’onda trascurata a livello mondiale, ha proprietà straordinarie: nella scala si frequenze da 1 a 70 Hz, esprime tutte le funzioni fisiologiche dell’essere umano e le può regolare in maniera endogena, senza effetti collaterali.
Dal sonno, indotto dalle bassissime frequenze, che attivano in ogni cellula le proteine PER e TIM regolatrici del sonno e dei ritmi circadiani, per la scoperta delle quali è stato assegnato il premio Nobel 2017 a tre grandi scienziati. Il campo elettromagnetico su tutto il corpo, uniformemente fa oscillare tutte le cellule, inducendo il sonno e destrutturando eccessi di adrenalina e ormoni dello stress. Il premio Nobel per la Medicina e la Fisiologia 2017 è stato assegnato a Jeffrey C. Hall, Michael Rosbash e Michael W. Young per le loro scoperte sui meccanismi molecolari che controllano i ritmi circadiani.
Questo premio Nobel è stato annunciato, in modo molto aulico ed evocativo, come il massimo punto di incontro tra la fisiologia degli organismi terrestri e l’astrofisica. Tutti gli esseri viventi che abitano il nostro pianeta devono infatti fare i conti con il ritmo giorno e notte, luce e oscurità e con lo scorrere delle stagioni, che dipendono dalla rotazione e rivoluzione della Terra.
Gli esseri viventi hanno sviluppato un meccanismo, che possiamo chiamare “orologio interno”, che li aiuta a prevedere e regolare la vita nelle varie parti della giornata controllando funzioni critiche come comportamento, livelli ormonali, sonno, temperatura corporea e tutto il metabolismo. Questo meccanismo è denominato sistema (o ritmo) circadiano.
I primi studi sull’orologio interno furono condotti sulle piante e sulla drosofila, il moscerino della frutta, organismo modello per eccellenza in genetica. Negli anni ’70 fu identificato proprio nella drosofila un gene, che, quando mutato, danneggiava il funzionamento del sistema circadiano. Il gene fu denominato period.
Bisognava ancora scoprire, però, come questo gene potesse influire sull’orologio interno.
Nel 1984, Jeffrey Hall e Michael Rosbash riuscirono a isolare il gene period e scoprirono che era responsabile per la codifica di una proteina detta PER, che si accumula durante la notte e si degrada durante il giorno con una modalità di accumulo/degradazione che segue un ciclo di 24 ore, in sincronia con il ritmo circadiano. Il successivo passo era capire come la proteina PER potesse regolare l’attività del gene period e quindi autoregolare la propria produzione. Il sistema non era così semplice come lo ipotizzavano Hall e Rosbash ma Michael Young nel 1994 fece luce sul meccanismo, scoprendo altri due geni coinvolti in questo affascinante processo: il gene timeless (TIM) e il gene doubletime (DBT). Le proteine TIM e DBT regolano il trasporto di PER all’interno del nucleo cellulare e ne modulano finemente la regolazione durante le 24 ore del ciclo circadiano. LA PROTEINA – Hall e Rosbash hanno poi scoperto che ‘Per’, la proteina codificata dal gene ‘period’, si accumula durante la notte e degrada durante il giorno. E che in pratica i suoi livelli oscillano durante le 24 ore in sincronia con il ritmo circadiano.
LA CELLULA
L’obiettivo fondamentale successivo fu quello di capire come queste oscillazioni circadiane potessero essere generate e sostenute. Jeffrey Hall e Michael Rosbash hanno quindi ipotizzato che la proteina ‘Per’ bloccasse l’attività del gene ‘period’. Ma, per farlo, la stessa proteina, prodotta nel citoplasma, deve raggiungere il nucleo della cellula, dove si trova il materiale genetico.
GENE ‘TIMELESS’
Come è possibile che riesca a farlo? A chiarirlo nel 1994 fu Young, che scoprì un secondo gene – ‘timeless’ (‘senza tempo’) – che codifica la proteina detta ‘Tim’, sempre essenziale per il mantenimento del normale ritmo circadiano. Lo scienziato mostrò che quando ‘Tim’ si lega a ‘Per’, le due proteine sono in grado di entrare nel nucleo cellulare e di bloccare l’attività del gene ‘period’.
LE OSCILLAZIONI
Questo meccanismo spiegava come si crea l’oscillazione dei livelli di proteine nella cellula, ma cosa controlla la frequenza delle oscillazioni? Michael Young ha identificato un ennesimo gene, ribattezzato ‘doubletime’ (‘doppio tempo’), che codifica la proteina Dbt, la quale ritarda l’accumulo della proteina ‘Per’. Questo ha chiarito come l’oscillazione viene regolata per aderire al ciclo delle 24 ore.
LA SINCRONIZZAZIONE
Successivamente, i premi Nobel hanno compiuto altre scoperte sulle componenti molecolari dell’interessante meccanismo, ad esempio quella sulla presenza di altre proteine necessarie per l’attivazione del gene ‘period’ e del meccanismo con cui la luce riesce a sincronizzare il nostro orologio interno. I loro studi hanno dunque contribuito a generare un vastissimo campo di ricerca, con ricadute concrete sulla nostra salute. Una curiosità: il termine ‘ritmo circadiano’ deriva dai termini latini (circa diem) che significano ‘intorno’ e ‘giorno’.
Un’altra scoperta, credo rilevante, fatta dalle mie ricerche, è la stimolazione muscolare senza elettrostimolazione, che potrebbe essere dannosa con le contrazioni, dato che muscoli e cervello sono collegati da recettori e motoneuroni.
Le fibre muscolari a contrazione lenta rosse, vengono usate in azioni muscolari di lunga durata Le fibre rosse trattengono più glicogeno e concentrano gli enzimi associati al metabolismo aerobico. I mitocondri sono più numerosi e di dimensioni maggiori, così come il numero di capillari che irrora la singola fibra. La ridotta dimensione facilita la diffusione dell’ossigeno dal sangue ai mitocondri, a causa della minor distanza che li separa. E’ l’abbondante contenuto di mioglobina e mitocondri a conferire a queste fibre il colorito rosso, da cui deriva il loro nome.
Si apre un nuovo capitolo per potenziare la forza muscolare a tutte le persone allettate, non solo agli sportivi .in maniera naturale, cedendo energia ATP, dal mitocondrio cellulare alla fibra muscolare, attraverso il canale della mioglobina, il secondo veicolo di ossigenazione dopo l’emoglobina.
Ho realizzato un materassino notturno confortevole che contiene tanti solenoidi che coprono uniformemente l’intero corpo umano.
La rigenerazione ossea oramai è validata e in quattro mesi le persone con osteoporosi possono verificare con la MOC DEXA il blocco o inversione della demineralizzazione ossea.
Il protocollo della Nasa del 1973 finalmente ha avuto giustizia e innovazione. Con l’uso notturno cresce il GH ormone della crescita fisiologico endogeno e migliora la rigenerazione di ossa, tendini, nervi e cartilagine.
I dispositivi medici da me progettati hanno tutte queste innovazioni, validate con pubblicazioni scientifiche come nel caso dell’osteoporosi, mentre sono in corso pubblicazioni su ansia e sonno e potenziamento muscolare delle persone allettate.
Sono contrario ai brevetti e le innovazioni in sanità dovrebbero essere di pubblico dominio.
Questi i miei recapiti per chiunque volesse informazioni o assistenza clinica e scientifica su OSTEOPOROSI, ARTROSI, INSONNIA, DEBOLEZZA MUSCOLARE, PROBLEMI POSTURALI.
Ognuno ha un contenuto d’acqua e una impedenza specifica e l’intensità del campo magnetico va tarata sulla singola persona.
danieleromano15@gmail.com
3452361039 3384843618
La mioglobina è stata la prima proteina di cui è stata determinata la struttura, fissa l’ossigeno che deve essere usato nei muscoli
La prima proteina
Qualsiasi discussione sulla struttura delle proteine deve cominciare necessariamente con la mioglobina, perché è stata la prima proteina di cui si è determinata la struttura.
John Kendrew e il suo gruppo, dopo anni di intenso lavoro, hanno determinato la struttura atomica della mioglobina ponendo così le fondamenta per una nuova era di comprensione della biologia.
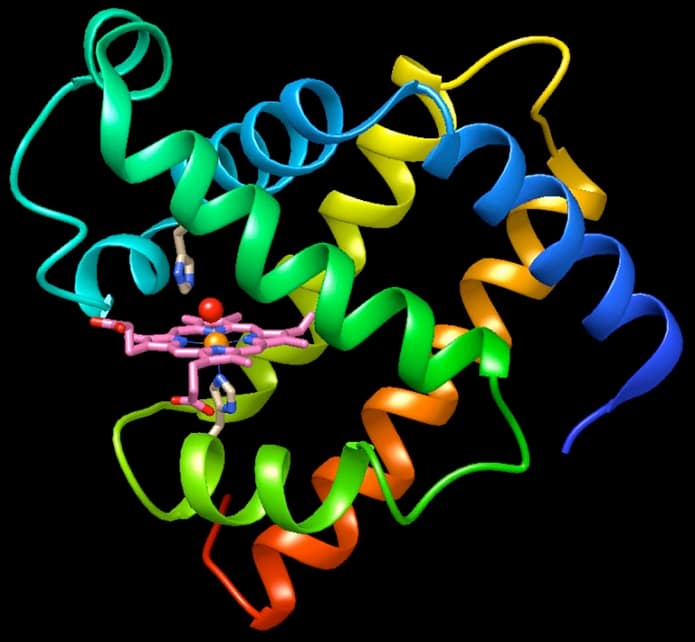
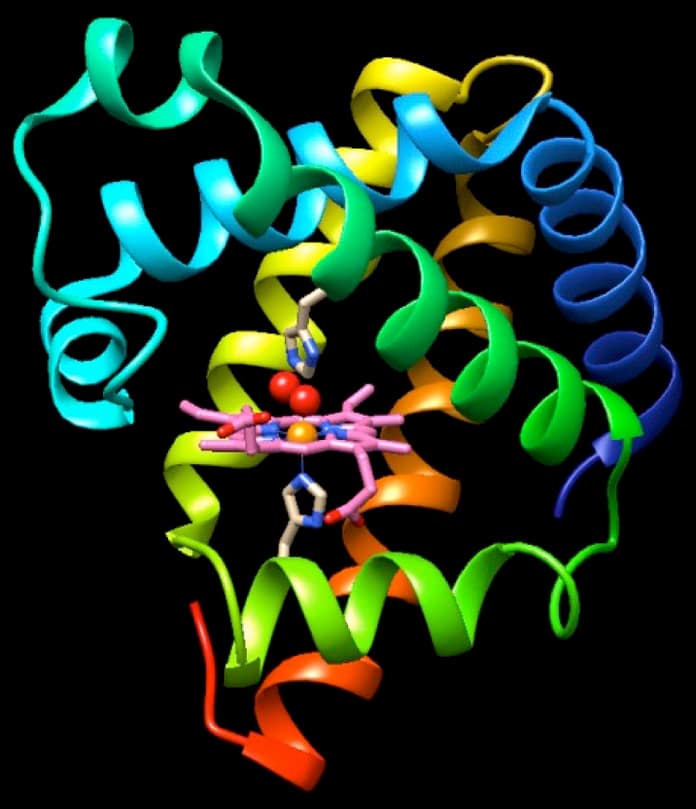
Questa struttura storica è mostrata nelle due immagini qui a fianco e qui sotto (file PDB 1mbn). Se osservate nel dettaglio questa molecola, ne rimarrete affascinati, proprio come lo fu il mondo nel 1960, nel vedere per la prima volta il meraviglioso intreccio di una proteina.
Mioglobina e muscoli
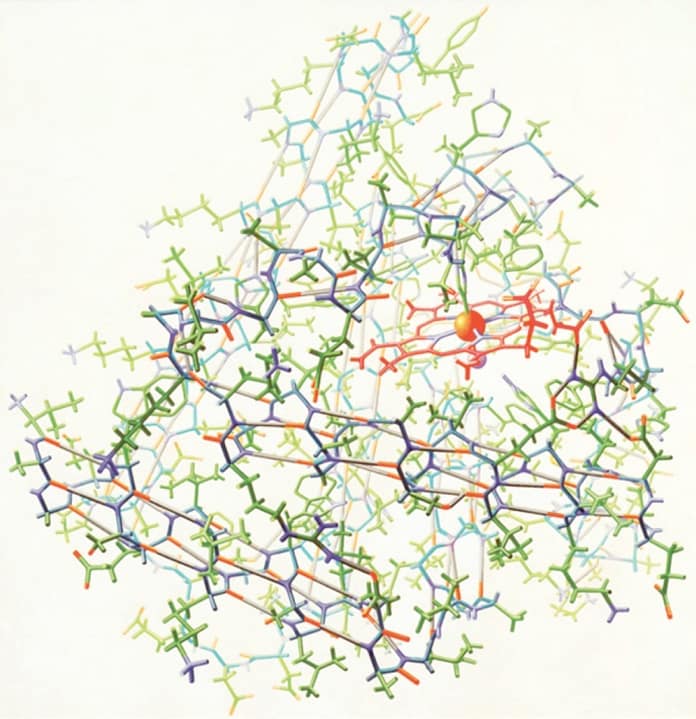
La mioglobina è una proteina piccola e rossa. È molto comune nelle cellule muscolari e dà alla carne il caratteristico colore rosso. Il suo compito è immagazzinare ossigeno O2, che viene usato quando i muscoli devono contrarsi intensamente. Per fare questo usa uno strumento chimico molto particolare, il gruppo eme, che le consente di catturare le sfuggenti molecole di ossigeno. L’eme è una molecola a forma di disco, mostrata in rosa nelle due figure qui sopra e a lato. Ha un foro al centro dove lega un atomo di ferro (arancione) ed è questo che riesce a legare l’ossigeno O2. In realtà, in questa molecola, il ferro dell’eme non sta legando i due atomi di ossigeno della molecola O2, ma lega un singolo atomo di ossigeno (rosso) di una molecola d’acqua. Questo è comunque sufficiente per darci un’idea della posizione che assume O2 quando si lega all’eme. Il gruppo eme si trova in una tasca sottile e profonda sul fianco della proteina, trattenuto in posizione da due istidine (amminoacidi con un anello a cinque atomi con due atomi di azoto blu) disposte una sopra e l’altra sotto il ferro. Rappresentare le strutture Quando è stata risolta la struttura della mioglobina, agli scienziati si è posto un problema molto complesso. La struttura era così grande che hanno dovuto inventare nuovi metodi per rappresentarla in modo soddisfacente. John Kendrew ha costruito un grande modello di fil di ferro della mioglobina basandosi sui dati sperimentali di densità elettronica. Poi è stato dato l’incarico ad un artista, Irving Geis, di realizzare un’immagine della mioglobina. Egli ha realizzato l’immagine mostrata qui a destra che è stata usata per illustrare un articolo su Scientific American. La grafica 3D computerizzata sarebbe stata inventata solo molti anni dopo, quindi egli ha dovuto creare questa immagine completamente a mano.
Mioglobina e balene
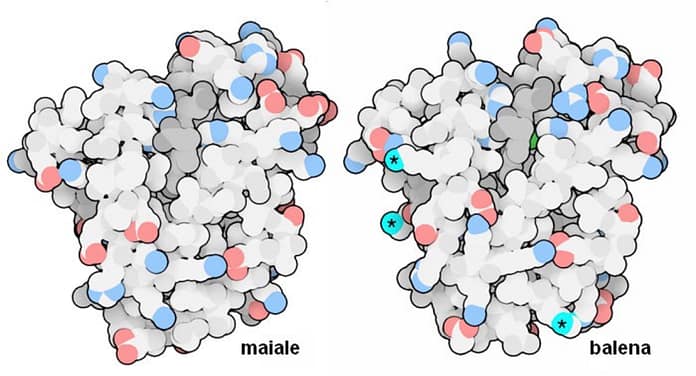
La mioglobina di John Kendrew (file PDB 1mbn) è stata ottenuta dai muscoli spermatici di balena. Balene e delfini hanno un grande bisogno di mioglobina per poter immagazzinare più ossigeno per le loro profonde immersioni sottomarine. Le balene hanno una quantità di mioglobina circa 30 volte maggiore degli animali terrestri. Uno studio recente ha rivelato che per accumulare tutta questa mioglobina hanno dovuto modificarne leggermente la struttura. Confrontando la mioglobina di maiale (file PDB 1pmb) con quella di balena (file PDB 1mbn) si nota che sulla seconda ci sono state alcune mutazioni che hanno introdotto amminoacidi carichi positivamente sulla superficie (evidenziati nella figura con un asterisco).
Gli animali marini hanno bisogno di queste cariche positive in più sulla superficie della loro mioglobina per creare forze repulsive tra le molecole vicine ed impedire così che la grande concentrazione di mioglobina ne causi l’aggregazione.
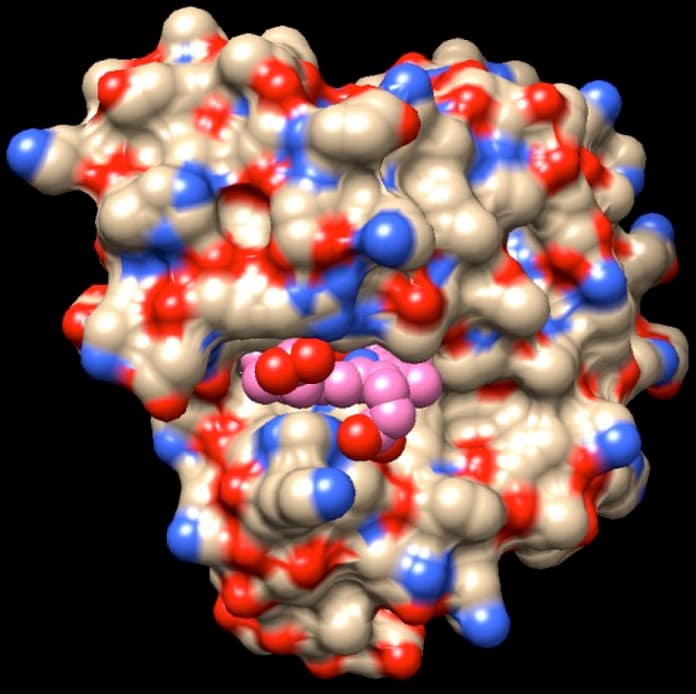
Ossigeno legato alla mioglobina
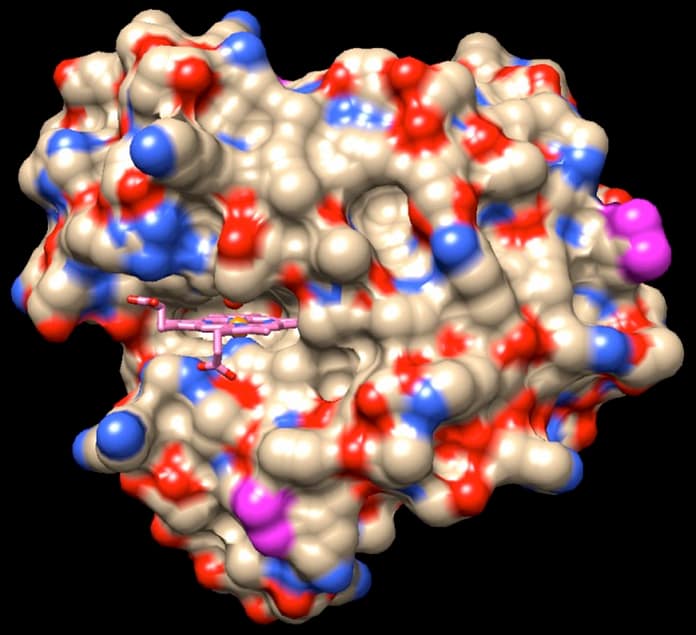
La struttura originale della mioglobina determinata da John Kendrew, al posto dell’ossigeno biatomico O2 legato al ferro, ha una molecola di acqua visibile come una sfera rossa sopra il ferro dell’eme nell’immagine iniziale. Qui sotto è mostrata una struttura più recente di mioglobina (file PDB 1mbo) che contiene invece ossigeno O2 (rosso). Confrontate le due figure. Nella prima figura, la catena proteica della mioglobina è rappresentata con un nastro, e quindi si può vedere facilmente l’ossigeno O2 (rosso) legato all’atomo di ferro (arancione) al centro del gruppo eme. Ma quando, come nella seconda figura, sono rappresentati anche tutti gli atomi della proteina, l’ossigeno scompare, nascosto all’interno della tasca. Come può l’ossigeno entrare e uscire, se è totalmente circondato dalla proteina? In realtà, la mioglobina (come tutte le molecole) non è mai ferma, ma compie piccoli movimenti di espansione, contrazione e torsione. Aperture provvisorie appaiono e scompaiono in continuazione e permettono all’ossigeno di entrare e uscire. La struttura mostrata qui è soltanto un’immagine istantanea della proteina, realizzata quando questa è nella forma ermeticamente chiusa. La vera struttura della proteina, invece, è dinamica, ma questi movimenti li possiamo solo immaginare.
Mioglobina
Proteina presente nelle fibre muscolari dei Mammiferi e dei Vertebrati. Il suo compito è sia di immagazzinare ossigeno, sia di aumentare la sua velocità di diffusione nelle cellule muscolari. È una proteina globulare coniugata a un gruppo eme, identico, quindi, a quello presente nell’emoglobina.
Il gruppo eme, contenente l’atomo di ferro ferroso, è situato in una tasca della molecola di m.; il resto dell’eme è dentro la molecola, circondato da residui non polari, tranne le 2 istidine, a una delle quali (detta residuo F8) è legato direttamente. L’atomo di ferro si trova circa 0,3Å fuori dal piano dell’eme stesso, spostato verso l’istidina F8; l’altra istidina (detta residuo E7) si trova molto vicina, ma non è legata al gruppo eme. Il sito che si combina con l’ossigeno è dall’altra parte del piano dell’eme e occupa solo una piccola parte del volume della m.; infatti, l’ossigeno si lega direttamente solo all’atomo di ferro dell’eme. Il suo sito di legame ha una spiccata caratteristica non polare, che esclude l’acqua dall’ambiente interno della molecola e protegge il Fe2+ dell’eme dall’ossidazione. È possibile distinguere 3 forme fisiologiche della m., con conformazione molto simile tranne che per il legame che l’atomo di ferro intraprende con diverse sostanze: ferrimioglobina, desossimioglobina e ossimioglobina (la forma legata all’ossigeno).
Rispetto all’emoglobina, la m. non è una proteina allosterica, presenta un’affinità per l’O2 indipendente dal pH e maggiore di quella dell’emoglobina. La conseguenza diretta di questa diversa affinità per l’O2 è che la m. è in grado di accettare ossigeno dall’emoglobina e immagazzinarlo nelle cellule muscolari. Infatti, durante la contrazione muscolare, quando la richiesta di ossigeno è massima e la pressione parziale di ossigeno intracellulare diminuisce, l’O2 si dissocia dalla m. e diviene disponibile per le reazioni di ossidazione del metabolismo cellulare.
Nell’uomo, la m. è particolarmente abbondante nei muscoli scheletrici e nel muscolo cardiaco. La presenza di m. nel sangue è detta mioglobinemia. La sua presenza patologica nelle urine è la mioglobinuria, che può verificarsi in seguito a violenti sforzi fisici (marce prolungate, mioglobinuria da marcia), nella malattia del Haff, in caso di gravi traumi delle masse muscolari (mioglobinuria traumatica) e nella cosiddetta mioglobinuria paralitica spontanea, rara e grave malattia febbrile, a cause ignote, con degenerazioni muscolari acute e paralisi flaccide.